
据国家药监局网站消息,5月23日,国家药品监督管理局、国家卫生健康委员会共同发布优化药品注册审评审批有关事宜的公告。
此次的公告一共提出五项最新事宜,明确提出要提高创新药上市审批效率,科学简化审批程序。
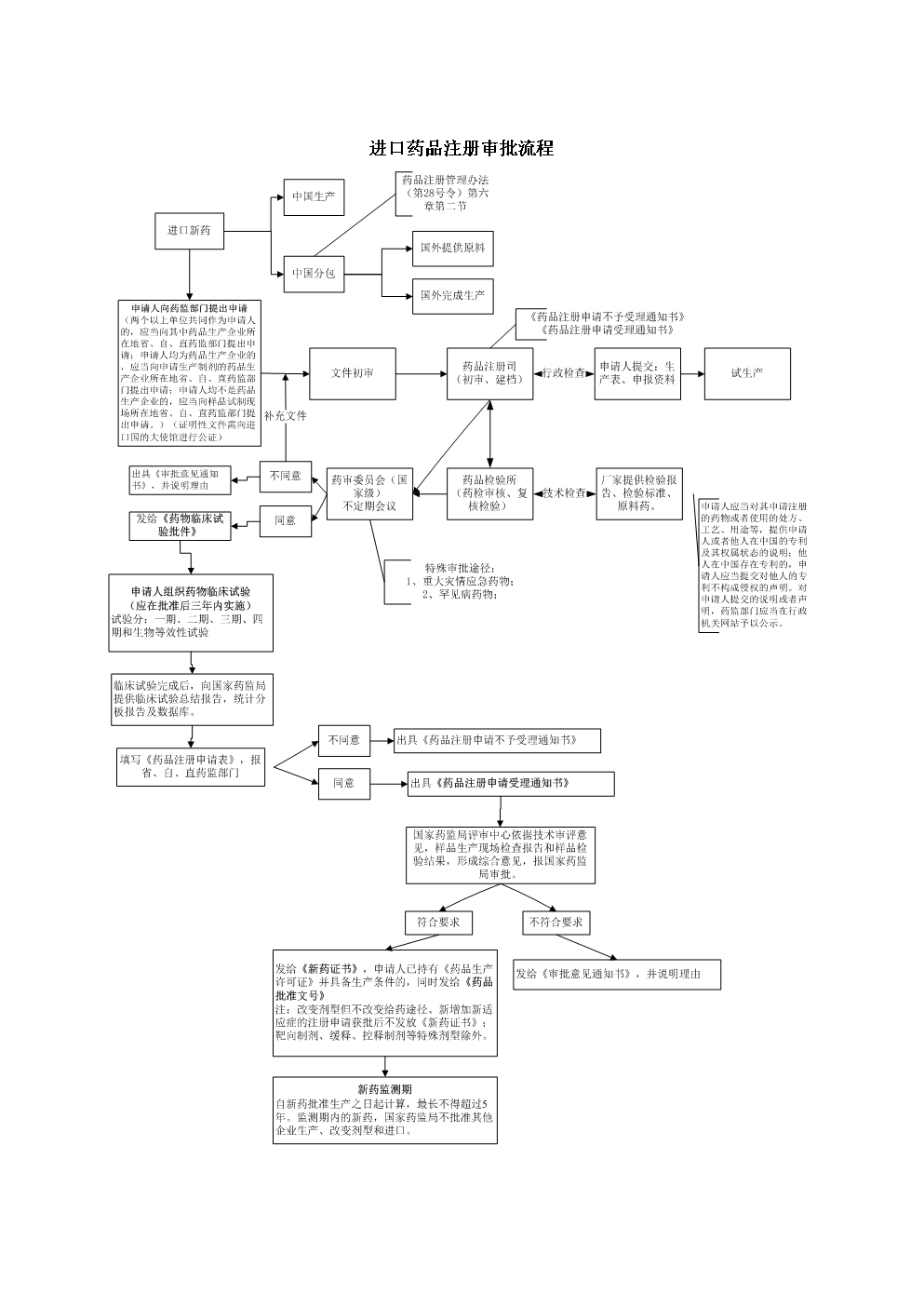
公告称,对于境外已上市的防治严重危及生命且尚无有效治疗手段疾病以及罕见病药品,进口药品注册申请人经研究认为不存在人种差异的,可以提交境外取得的临床试验数据直接申报药品上市注册申请。对于本公告发布前已受理并提出减免临床试验的上述进口药品临床试验申请,符合《药品注册管理办法》及相关文件要求的,可以直接批准进口。
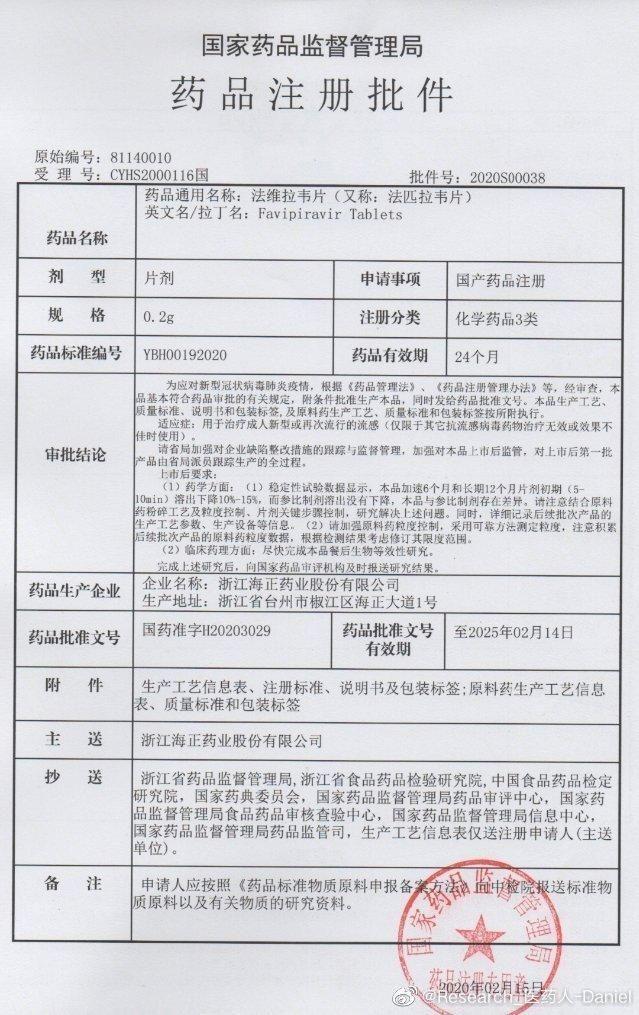
平安证券分析认为,该规定将大大缩短国外新药在国内上市时间,提高国内对于全球创新药的可及性。以前国外上市的进口药进入我国销售,须在国内再次进行新药临床试验,这个阶段耗时2年以上,且需要投入一笔不小的费用,导致国内可用的全球创新药远远少于国外。据统计,2016年7月之前,美国食品药品监督管理局一共批准了43个小分子靶向药物,其中仅有13个在中国上市。
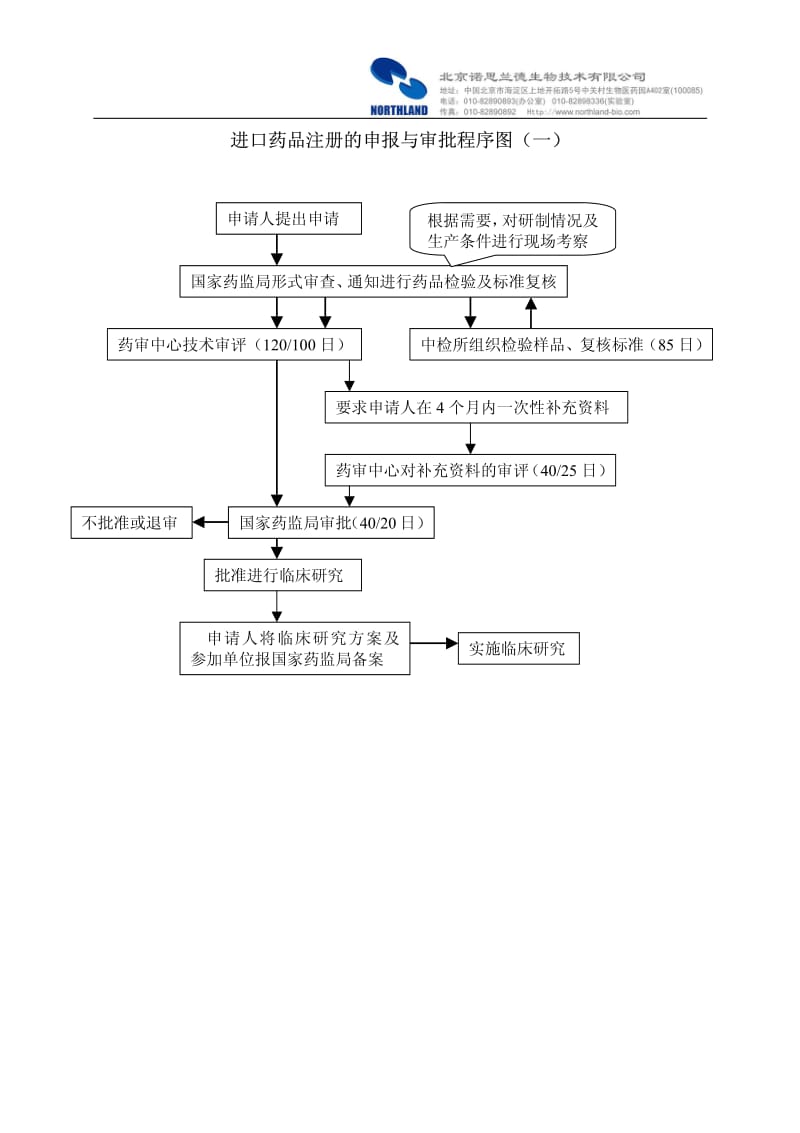
平安证券表示,该规定出台后,符合条件的药品不需要再次进行临床试验,相当于降低了中国市场的进入壁垒,会有更多的创新药企业主动申报产品进入中国,国内做进口药品代理的公司也将加大对进口创新药的引进力度。

公告明确,取消进口药品再注册核档程序,进口药品再注册申请受理后,全部资料转交药审中心审评审批。对于本公告发布前已受理的进口药品再注册申请,包括进口再注册核档意见为无需质量标准复核的注册申请,统一转入药审中心进行审评审批。将目前由国家药品监督管理局作出的各类临时进口行政审批决定去美国上市需要国内审批吗,调整为由药审中心以国家药品监督管理局名义作出。
对此,平安证券点评道,该公告之前,申请临床试验的某些类别的产品需要出具检验报告,此次改为经药审中心评估认为无需检验的,就可以免掉这一步。进口药品再注册的核档程序在中检院去美国上市需要国内审批吗,官方规定是40个工作日,实际耗时更长。此次规定省去这一步,将切实缩短审评审批时间。
有分析认为,本次这一公告的落地实施,将进一步改善中国患者此前无望用上最新药物的困境。同时,随着中国越来越多地参与到国际多中心药物临床试验中,进口新药可在国内外同步递交临床试验申请,国际多中心药物临床试验后,药品可直接申请在中国上市。这一系列提速“救命药”的改革后,重复实验减少,上市效率提高,急需的新药有望更快进入中国。
更多财税咨询、上市辅导、财务培训请关注Z6尊龙官网咨询官网 素材来源:部分文字/图片来自互联网,无法核实真实出处。由Z6尊龙官网咨询整理发布,如有侵权请联系删除处理。








 400-835-0088
400-835-0088
